KEMIJA 8. razred
Urednik strani: Antonija Brozovič elektronski naslov: toncka.brozovic@os-trebnje.si
Naslovi spletnih strani, ki jih lahko uporabite pri delu in učenju na daljavo:
- http://www.osbos.si/ekemija/e-gradivo/
- https://eucbeniki.sio.si/kemija8/index.html
- http://www.kii3.ntf.uni-lj.si/e-kemija/mod/resource/view.php?id=28
__________________________________________________________________________________________________________________________
10. teden (25. 5. 2020 – 29. 5. 2020)
Ta teden končujemo z vsebinskim sklopom ELEMENTI V PERIODNEM SISTEMU. Predelamo še učno snov o NEKOVINAH.
Potek dela ta teden:
Anketa-reši jo šele, ko predelaš učno snov tega tedna:
ANKETA- ELEMENTI V PERIODNEM SISTEMU
I. Ogled posnetka z razlago.
NEKOVINE
II. Preberi učno snov v učbeniku (str. 109-113)
III. Zapis v zvezek

__________________________________________________________________________________________________________________________
IV. Anketa: povezava na vrhu 10 tedna
9. teden (18. 5. 2020 – 22. 5. 2020)
Še dve uri bomo obravnavali elemente v periodnem sistemu. Ta teden bomo spoznali prehodne elemente. Naredili boste tudi domači poskus.
I. OBRAVNAVA NOVE SNOVI
V učbeniku (str. 105-108) preberi snov o prehodnih elementih. Prehodni elementi in njihove spojine so zelo pomembni v našem življenju. Med prehodnimi elementi je zelo pomembno železo, pa tudi nekateri drugi- zlato, baker, cink, platina,…
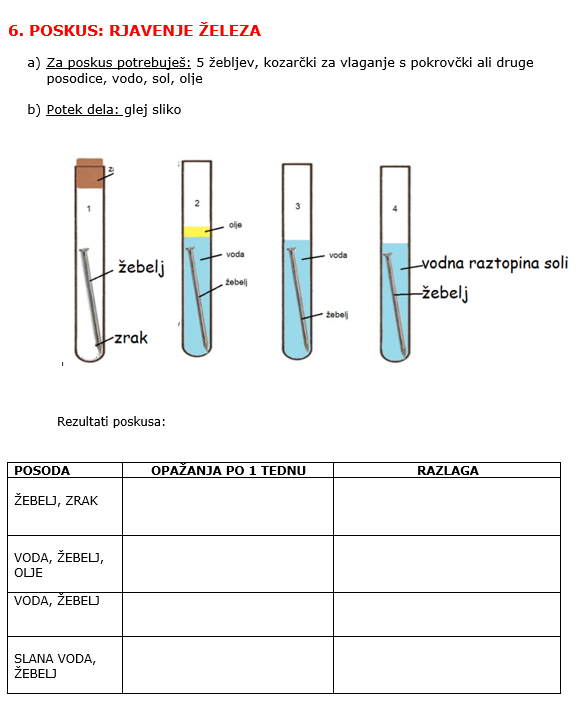
Poglej si slikce. Naredi zapis v zvezek. Naredi poskus in zapiši opažanja. Poslikaj rezultate poskus in slike shrani.


II. ZAPIS V ZVEZEK IN POSKUS
Lahko si pogledaš tudi v wordovih dokumentih:8. teden prehodne kovine, prehodne kovine
Naredi zapis v zvezek. V enem tednu izvedi poskus. Zapiši opažanja poskusov. Poslikaj poskuse po 5 dneh od nastavitve in shrani slikco.
________________________________________________________________________________________________________________________
8. teden (11. 5. 2020 – 15. 5. 2020)
I. OBVESTILO O OCENJEVANJU
Zagotovo vas zanima, kako bo z ocenjevanjem. Ker ste v mesecu februarju in marcu dobili ustno in pisno oceno, sedaj z ocenjevanjem ne bomo hiteli. Verjetno imate veliko dela z drugimi predmeti, kjer še niste imeli ocen.
Jaz skrbno pregledujem vaše oddane naloge in jih vrednotim. Eno oceno načrtujem pridobiti z vrednotenjem vašega dela na daljavo kot celote ( odzivnost, vračanje nalog, pravilnost rešenih nalog). Moram reči, da večina učencev oddaja ankete. Tako odzivnost pričakujem tudi naprej.
Od vas pričakujem tudi, da si redno delate zapiske. Drugo šolsko leto boste zapiske v zvezku še potrebovali.
II. RAZLAGA NOVE SNOVI
Povezava do videoposnetka :
https://video.arnes.si/portal/asset.zul?id=oMglSdFGWKhnsRRLJYTJcovw
Povezava do videoposnetkov kemijskih reakcij, ki so omenjeni v razlagi:
LASTNOSTI NATRIJA:
https://eucbeniki.sio.si/kemija1/496/index.html (ena stran naprej v i ucbeniku)
REAKCIJE ALKALIJSKIH KOVIN Z VODO
https://eucbeniki.sio.si/kemija8/952/index2.html
REAKCIJA KALCIJA Z VODO:
https://www.youtube.com/watch?v=V9mPJ4znoks
https://www.youtube.com/watch?v=-_0UiO61GPc
GORENJE MAGNEZIJA:
https://www.youtube.com/watch?v=VtgcCCxZTjs
PLAMENSKE REAKCIJE:
https://www.youtube.com/watch?v=K6PwoH-zxqc
III. ZAPIS V ZVEZEK

_________________________________________________________________________________________________________________________
7. teden (4. 5. 2020 – 8. 5. 2020)
Pa smo spet nazaj. Do konca šolskega leta moramo obravnavati še vsebinski sklop ELEMENTI V PERIODNEM SISTEMU in pridobiti še kakšno oceno. Zdaj pa kar na delo, lepo po vrsti.
I. REŠITVE 6. TEDNA
Preglej rešitve in v zvezku popravi napake z rdečim pisalom.



II. NOVA SNOV
Začeli bomo z obravnavo novega vsebinskega sklopa ELEMENTI V PERIODNEM SISTEMU. V tem poglavju boste spoznali lastnosti, uporabo različnih skupin kemijskih elementov. O kovinah ste veliko novega spoznali pri TEHNIKI.
Pri delu uporabljaj učbenik (str. 92.- 114), e-ucbenik
- Viri elementov in spojin v naravi
- Preberi učno snov v učbeniku (učb. str. 92-93)
- Preberi učno snov v e-ucbeniku ( https://eucbeniki.sio.si/kemija8/948/index.html str.139.- 143)
2. Kovine
- Preberi učno snov v učbeniku (97.-99 in 105-108)
- Preberi učno snov v e- ucbeniku (https://eucbeniki.sio.si/kemija8/952/index.html)
III. ZAPIS V ZVEZEK


__________________________________________________________________________________________________________________________
PRVOMAJSKE POČITNICE (27. 4. 2020- 3. 5. 2020)
Pred nami so počitnice, sicer malo drugačne kot druga leta. Učenci, ki ste resno in redno opravljali šolske obveznosti, zdaj je čas za počitek. Ankete opravljajte skrbno, saj bodo le te del ocene, ki jo boste dobili v maju.
V tednu po počitnicah boste imeli naravoslovni dan.
Pa srečno in zdravo na počitnicah.
A. Brozovič
___________________________________________________________________________________________________________________
6. teden (20. 4. 2020- 24. 4. 2020)
Že smo v zadnjem delovnem tednu pred prvomajskimi počitnicami. Kar spomnite se, kako smo prejšnja leta komaj čakali teh počitnic. Zdaj pa komaj čakamo, da ponovno pridemo v šolo.
Lepe počitnice vam želim.
A. Brozovič
I. ANKETA
S to anketo boš pokazal poznavanje in razumevanje učne snovi celega vsebinskega sklopa. A ne prehitevaj.
Anketo boš lahko rešil šele, ko boš šel lepo po vrsti. Preberi točke: ANALIZA ANKETE, REŠITVE 5. TEDNA, DELO ZA 6. TEDEN. Ko boš s pomočjo zapiskov v zvezku rešil naloge za preverjanje in utrjevanje, se lahko lotiš reševanja ankete. Anketa je za vse obvezna. Dostopna bo do petka, 24. 4. 2020. Vaše rešitve bom skrbno pregledala, ugotovitve si bom zapisala.
Povezava do ankete:
https://www.1ka.si/a/275103
II. ANALIZA ANKET
Ankete sem pregledala in ugotovila, da večina učencev razume temeljne pojme. 89% učencev je oddalo obe anketi, 4 učenci niso oddali nobene ankete.
III. REŠITVE 5. TEDNA- ZAPIS V ZVEZEK

IV. DELO ZA 6. TEDEN
Prejšnji teden smo zaključili z obravnavo vsebinskega sklopa POVEZOVANJE DELCEV.
Temeljne vsebine, ki jih morate poznati:
DELCI, KI GRADIJO SNOV (atom, polarna molekula, nepolarna molekula, ion)
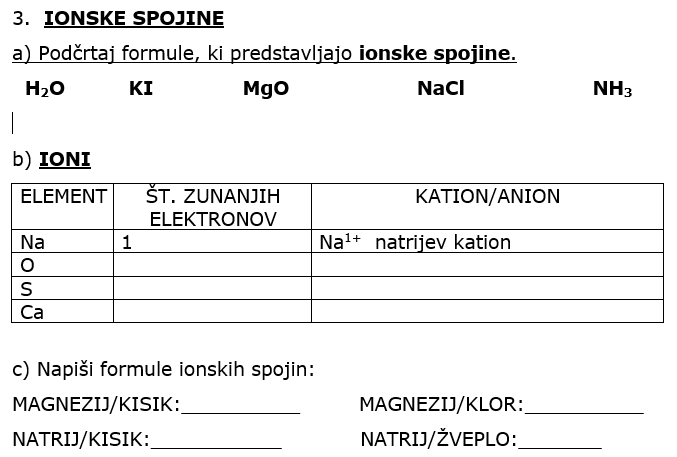
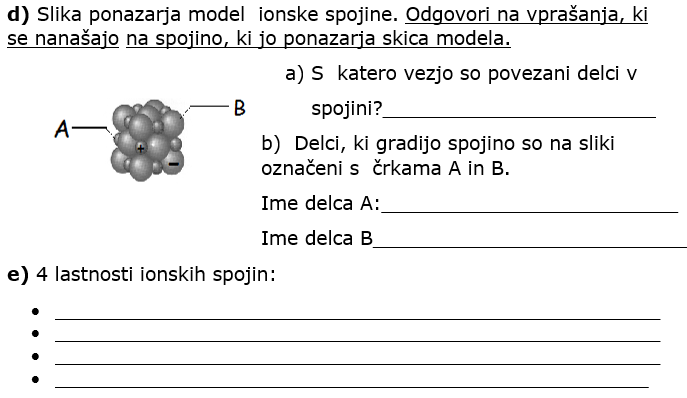
IONSKA VEZ, IONSKE SPOJINE (zgradba, lastnosti, formule ionskih spojin)
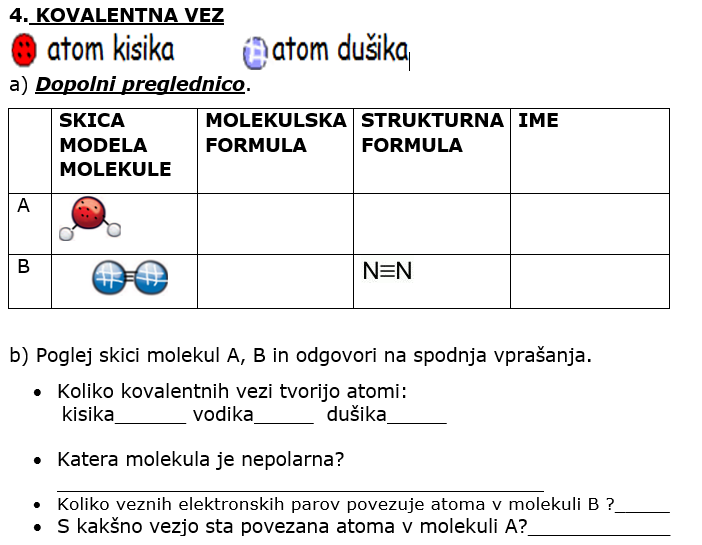
KOVALENTNA VEZ (polarna, nepolarna, lastnosti, zgradba)
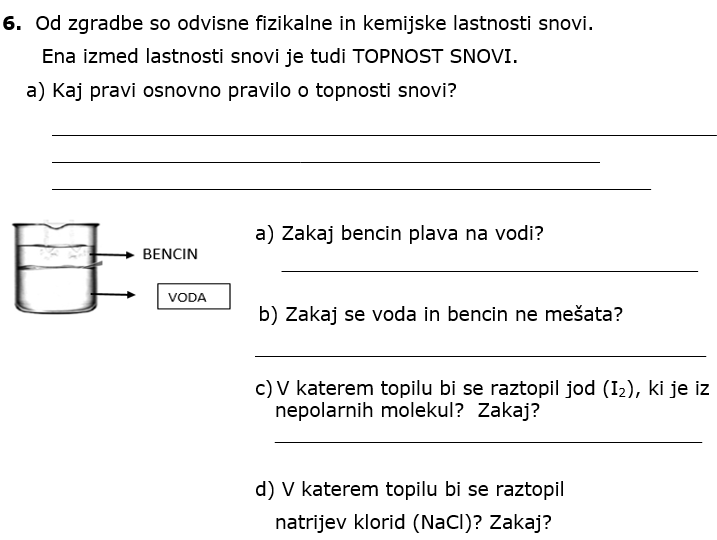
OSNOVNO PRAVILO O TOPNOSTI SNOVI
Preberi zapiske v zvezku (predvidevam, da imaš urejene), potem pa se loti reševanja nalog, s katerimi boš
utrdil osnovne pojme vsebinskega sklopa. Naloge lahko natisneš (če imaš to možnost), drugače pa prepiši v zvezek, reši, rešitve poslikaj in jih prilepi v anketo, ki jo imaš na vrhu 6. tedna.

__________________________________________________________________________________________________________________________
5. teden (13. 4. 2020- 17. 4. 2020)
I. Pozdravljam vas iz domače učilnice. Ta teden boste spoznali OSNOVNO PRAVILO TOPNOSTI SNOVI. Še prej pa preverimo osvojeno znanje in razumevanje snovi o KOVALENTNI VEZI. Predlagam vam, da vzamete zvezek in periodni sistem elementov. V zvezku natančno preberite zapiske o kovalentni vezi, potem pa se lotite reševanja.
PREVERJANJA ZNANJA: https://www.1ka.si/a/272306
Anketa je aktivna do petka, 17. 4. 2020
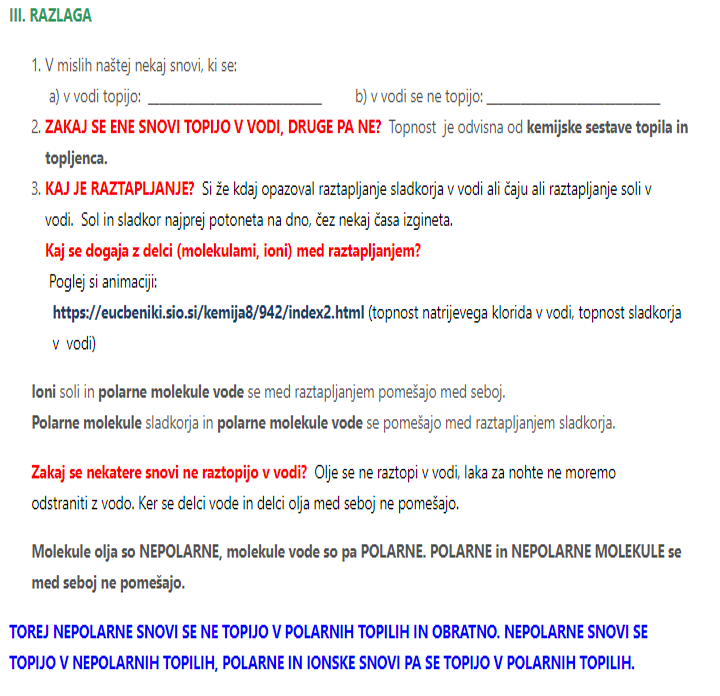
Animacija:
https://eucbeniki.sio.si/kemija8/942/index2.html (topnost natrijevega klorida v vodi, topnost sladkorja v vodi)
IV.ZAPIS V ZVEZEK
TOPNOST SNOVI IN OSNOVNO PRAVILO TOPNOSTI
- Raztapljanje je pojav, da se delci topljenca (ioni, molekule) pomešajo med delci topila (atomi, molekule).
TOPILO + TOPLJENEC → RAZTOPINA
2. Poskusi: raztapljanje snov polarnem in nepolarnem topilu
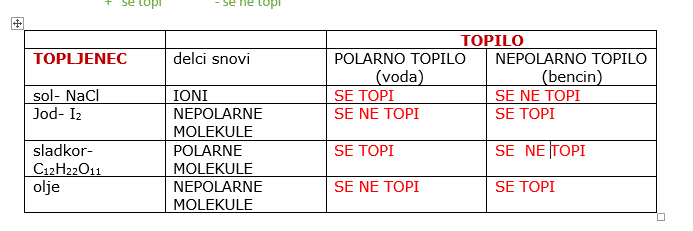
Preberi pravilo topnosti pod tabelo in predvidi rešitve raztapljanja: + snov se topi – snov se ne topi

- DOMAČI POSKUS:
a) V kozarec nalij vodo (do višine 5 cm), dodaj olje ( 1 cm). Z žlico vse skupaj premešaj in počakaj.
Kaj se zgodi? Nariši in opiši.
b) V isti kozarec nalij 1 brizg detergenta za pomivanje posode. Pomešaj z žlico.
Kaj se zgodi? Nariši in opiši.
Če želiš, lahko pogledaš wordov dokument: 5. TEDEN TOPNOST SNOVI IN OSNOVNO PRAVILO TOPNOSTI
___________________________________________________________________________________________________________________
4. teden (6. 4. 2020- 10. 4. 2020)
Zakorakali smo že v 4. teden učenja na daljavo. Ta teden boste preverili znanje o poznavanju ZGRADBE, LASTNOSTI, FORMULE IONSKIH SPOJIN. Anketo boste izpolnjevali vsak teden. Izpolnjevanje ankete je za vse učence obvezno. https://www.1ka.si/a/269698
Anketa je ativna od 6. 4. 2020- 10. 4. 2020. Rešitve ankete bodo na spletni strani v petek, 10. 4. 2020.
Rešitve preverjanja znanja o ionskih spojinah:
- Atom elementa žvepla ima 6 zunanjih elektronov.
2. Ionske spojine nastanejo s povezovanjem atomov kovin in nekovin.
3. Formule 4 ionskih spojin: FeS, MgO, NaCl, KBr, MgCl2,…
4. Pravilne trditve o ionih: ioni imajo pozitiven ali negativen naboj; ion nastane, ko atom odda ali sprejme
zunanje elektrone; kation nastane, ko atom odda zunanje elektrone
5. Simbol in ime iona klora: Cl1- (1- je napisana zgoraj) kloridni anion.
6. Simbol in ime iona natrija: Na1+ 8natrijev kation)
7. Gradniki ionskih spojin so kation in anioni.
8. Temperatura tališča ionskih spojin je visoka.
9. Slika ponazarja raztapljanje ionske spojine v vodi.
10. Ionske spojine prevajajo el. tok v talinah in v vodnih raztopinah.
V tej učni uri boste spoznali značilne lastnosti kovalentnih snovi.
Kovalentne snovi so snovi, ki so zgrajene iz molekul. Molekule so lahko nepolarne (nepolarna molekula ima oba pola enaka, npr O2, H2,…… Polarne molekule pa imajo različna pola- pozitivni in negativni pol- npr molekula vode.
Med nepolarnimi molekulami skoraj ni privlačnih sil, zato imajo te snovi nizka tališča in vrelišča. Med polarnimi molekulami pa so privlačne sile, vendar veliko šibkejše kot med ioni v ionskih spojinah.
Poglej posnetek poskusa na spletni strani. Poskus prikazuje, kako sta si dve navidez enaki spojini različni po lastnostih.
https://eucbeniki.sio.si/kemija8/942/index1.html
https://eucbeniki.sio.si/kemija8/942/index3.html
Povzetek učne snovi zapiši v zvezek in dopolni:
LASTNOSTI KOVALENTNIH SNOVI (Učbenik, str. 73)
- Primeri kovalentnih snovi:
a) elementi: O2, H2, S8, N2, P4, VII( F2, Cl2, Br2, I2)
b) kovalentne spojine: H2O, NH3, HCl, C6H12O6,…..
- Lastnosti kovalentnih snovi so odvisne od zgradbe.
Osnovni gradniki kovalentnih snovi so molekule (POLARNE MOLEKULE, NEPOLARNE MOLEKULE) med katerimi so šibke privlačne sile.
| LASTNOST | OPIS |
| AGREGATNO STANJE | trdno, tekoče, plinasto |
|
ELEKTRIČNA PREVODNOST
|
ne prevajajo |
| TALIŠČE, VRELIŠČE | nizki (zaradi šibkih privlačnih sil med molekulami |
| TOPNOST |
· Snovi, zgrajene iz polarnih molekul se dobro topijo v polarnih topilih (npr. v vodi), ne topijo pa se v polarnih topilih (npr. v bencinu). · Snovi zgrajene iz nepolarnih molekul se slabo ali ne topijo v polarnih topilih (npr. v vodi), dobro pa se topijo v nepolarnih topilih (npr. v bencinu). |
- Na spletni strani poišči podatke o lastnosti nekaterih kovalentnih snovi snovi.
| SNOV | VIDEZ- agregatno stanje, barva | TALIŠČE, VRELIŠČE |
| JOD- I2 | ||
| KISIK- O2 | ||
| VODA- H2O | ||
|
SLADKOR- SAHAROZA- C12H22O11
|
Natančnejšo razlago si lahko pogledaš tukaj:KEM8 4. TEDEN
__________________________________________________________________________________________________________________________
3. teden( 30. 3. 2020- 3. 4. 2020)
8. RAZRED
Upam, da vam gre delo na daljavo dobro od rok. Kako vam je uspel poskus PRIPRAVA DOMAČEGA KVASA? Naslednji teden vam bom pripravila anketo, v kateri bom preverila, kako nam gre delo na daljavo. Za ta teden sem pripravila naslednje: KEM83. TEDEN
__________________________________________________________________________________________________________________________
Pozdravljeni osmarji in devetarji. Upam, da vam je čas hitro tekel, da ste dobro opravili šolske obveznosti in da ste zdravi. Za 2. teden sem vam pripravila naslednje naloge.
- RAZRED– 2. TEDEN 23. 3.- 27. 3
Za ta teden sem vam pripravila 2 nalogi. Prva naloga je praktična, drugo nalogo pa zapišite v zvezek.
- naloga: PRIPRAVA DOMAČEGA KVASA
DOMAČI KVAS
Letošnje šolsko leto smo obravnavali KEMIJSKE REAKCIJE. Ena izmed kemijskih reakcij, ki poteka pri peki kruha je tudi reakcija alkoholnega vrenja. Pri tej kemijski reakciji je eden izmed produktov tudi plin OGLJIKOV DIOKSID, ki omogoča vzhajanje kruha. Pri pripravi testa nujno potrebujemo kvas.
Zaradi izbruha koronavirusa v številnih trgovinah ne moremo kupiti svežega kvasa, pa tudi suhi kvas je že pošel. Na spletu sem našla recept za pripravo domačega kvasa.
Potrebščine: čist litrski kozarec za vlaganje, 1,5 dl mlačne vode,
1 žlička sladkorja, 2 veliki žlici moke, 4 krhlje jabolka (z lupino)
Potek:
V velik steklen čist kozarec vlijemo 1,5 dl mlačne vode ter dodamo 1 žličko sladkorja in 2 veliki žlici moke. Premešamo, da zmes nima grudic, nato pa dodamo še 4 jabolčne krhlje brez pečk. Kozarec zapremo ter ga dva dni pustimo pri miru na sobni temperaturi. Poberemo ven jabolka in kvas je pripravljen. Količina kvasa, ki ga dobimo, zadostuje za dve peki kruha po 2 kilograma.
Predlagam ti, da narediš poskus in pridobljeni kvas uporabiš za pripravo kruha. O rezultatih boš poročal, ko se zopet vidimo v šoli, upam da čimprej.
- naloga: odpri wordov dokument KEMIJA8 2. teden
___________________________________________________________________________________________________________________
KEMIJA8– 1. TEDEN
KEM8
Odpri wordov dokument-KEM8. Prepiši snov in dopolni, kjer je to potrebno. Preberi učno snov v učbeniku.
Pomagaj si s spletnimi stranmi:
https://eucbeniki.sio.si/kemija8/index.html
http://www.kii3.ntf.uni-lj.si/e-kemija/mod/resource/view.php?id=286
KEM9
Odpri wordov dokument. Prepiši snov in dopolni, kjer je to potrebno. Preberi učno snov v učbeniku.
Pomagaj si s spletnimi stranmi:
https://eucbeniki.sio.si/kemija9/index.html
http://www.kii3.ntf.uni-lj.si/e-kemija/mod/resource/view.php?id=286
